Химические свойства альдегидов и кетонов
Ниже приведены реакции, которые встречаются в официальных пособиях по подготовке к ЕГЭ, а также на сайте ФИПИ.
1. Реакции присоединения
Гидрирование:
+ H2 кат. ([21], стр. 349)
+ H2 кат. ([21], стр. 336)
+ 2H2 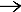 ([21], стр. 321)
([21], стр. 321)
В случае кетонов (в рамках школьной программы) рассматриваются только реакции гидрирования:
+ H2 кат. ([21], стр. 335)
2. Реакции окисления
1) Аммиачным раствором оксида серебра (Ag2O (NH3 р-р), реакция серебряного зеркала):
+ 4[Ag(NH3)2]OH t° (NH4)2CO3 + 4Ag + 6NH3 + 2H2O ([2], стр. 199)
+ 2[Ag(NH3)2]OH t° + 2Ag + 3NH3 + H2O ([21], стр. 42)
+ 2[Ag(NH3)2]OH t° + 2Ag + 3NH3 + H2O ([21], стр. 62)
+ 2[Ag(NH3)2]OH t° + 2Ag + 3NH3 + H2O ([21], стр. 357)
2) Свежеприготовленным гидроксидом меди (II):
+ 4Cu(OH)2 (голубой) t° CO2 + 2Cu2O + 5H2O ([2], стр. 200)
+ 2Cu(OH)2 (голубой) t° + Cu2O↓ (красный) + 2H2O ([21], стр. 23)
3) Окисление в щелочной среде:
+ 2KMnO4 + 3KOH 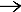 + 2K2MnO4 + 2H2O ([21], стр. 347)
+ 2K2MnO4 + 2H2O ([21], стр. 347)
+ 2KMnO4 + 3KOH 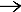 + 2K2MnO4 + 2H2O ([21], стр. 336)
+ 2K2MnO4 + 2H2O ([21], стр. 336)
+ 2NaMnO4 + 3NaOH 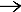 + 2Na2MnO4 + 2H2O ([21], стр. 333)
+ 2Na2MnO4 + 2H2O ([21], стр. 333)
+ 4KMnO4 + 6KOH 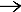 + 4K2MnO4 + 4H2O ([21], стр. 349)
+ 4K2MnO4 + 4H2O ([21], стр. 349)
4) Окисление в кислой среде:
5 + 4KMnO4 + 6H2SO4 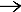 5 CO2 + 4MnSO4 + 2K2SO4 + 11H2O ([21], стр. 81)
5 CO2 + 4MnSO4 + 2K2SO4 + 11H2O ([21], стр. 81)
3 + K2Cr2O7 + 4H2SO4 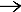 3 + K2SO4 + Cr2(SO4)3 + 4H2O ([21], стр. 121)
3 + K2SO4 + Cr2(SO4)3 + 4H2O ([21], стр. 121)
+ K2Cr2O7 + 4H2SO4 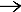 3 + K2SO4 + Cr2(SO4)3 + 4H2O ([21], стр. 229)
3 + K2SO4 + Cr2(SO4)3 + 4H2O ([21], стр. 229)
5 + 4KMnO4 + 6H2SO4 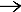 5 + 4MnSO4 + 2K2SO4 + 6H2O ([21], стр. 321)
5 + 4MnSO4 + 2K2SO4 + 6H2O ([21], стр. 321)
5 + 2KMnO4 + 3H2SO4 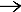 5 + 2MnSO4 + K2SO4 + 3H2O ([21], стр. 72)
5 + 2MnSO4 + K2SO4 + 3H2O ([21], стр. 72)
Страница создана в химическом редакторе.
